会议介绍
第13期 CRISPR/Cas9基因编辑技术(包含Base editor)学习班
2019/5/25-27(24号报到)
上海浦东中兴和泰酒店
医药加CRISPR/Cas9学习班简介
CRISPR/Cas9 是细菌和古细菌在长期选择压力中形成的一种适应性免疫防御,可用来有效抵御病毒及外源DNA的入侵。CRISPR的Type II已经被广泛用于基因工程,它包含Cas9,crRNA和tracrRNA,其中crRNA含有能够识别20bp的靶向互补序列。Cas9,crRNA和tracrRNA组成复合体,识别并结合crRNA互补的序列,然后解开DNA双链,Cas9中的HNH活性位点剪切crRNA的互补DNA链,RuvC活性位点剪切非互补链,最终导致DNA的双链断裂(DSB),进而实现基因的敲除和插入。
目前,CRISPR/Cas9系统已经广泛用于对哺乳动物细胞,细菌,斑马鱼,小鼠,猪,猴的基因编辑。本学习班将详细讲解CRISPR/Cas9基因编辑工具原理,操作流程,理论结合实践,将让大家详细了解到具体如何利用CRISPR/Cas9技术构建基因修饰动物等。学习班将为相关科研工作人员和兴趣爱好者提供了很好的培训资源。
学习预期:
1,掌握基因打靶与基因编辑技术(ZNF,TALENs,CRISPR/Cas9),能够设计sgRNA靶点,构建CRISPR/Cas9质粒,用于基因敲除和敲入。
2,掌握CRISPR/Cas9质粒转染方法, 阳性细胞克隆筛选方法体系,基因编辑细胞系的建立,基因修饰情况分析方法。
3,掌握CRISPR/Cas9脱靶产生的原因,脱靶检测方法,降低脱靶问题的方法
4,掌握CRISPR/Cas9的实际应用,对构建基因修饰小鼠和基因修饰大动物(猪)有较深入了解。
5,掌握新基因编辑工具,如:Cpf1, C2C2, base editing等。
6,掌握基因编辑研究领域前沿进展,基因编辑工具的拓展应用、临床应用等,形成利用基因编辑工具结合自己研究内容等科学思维。
7. Base editor 使用方法
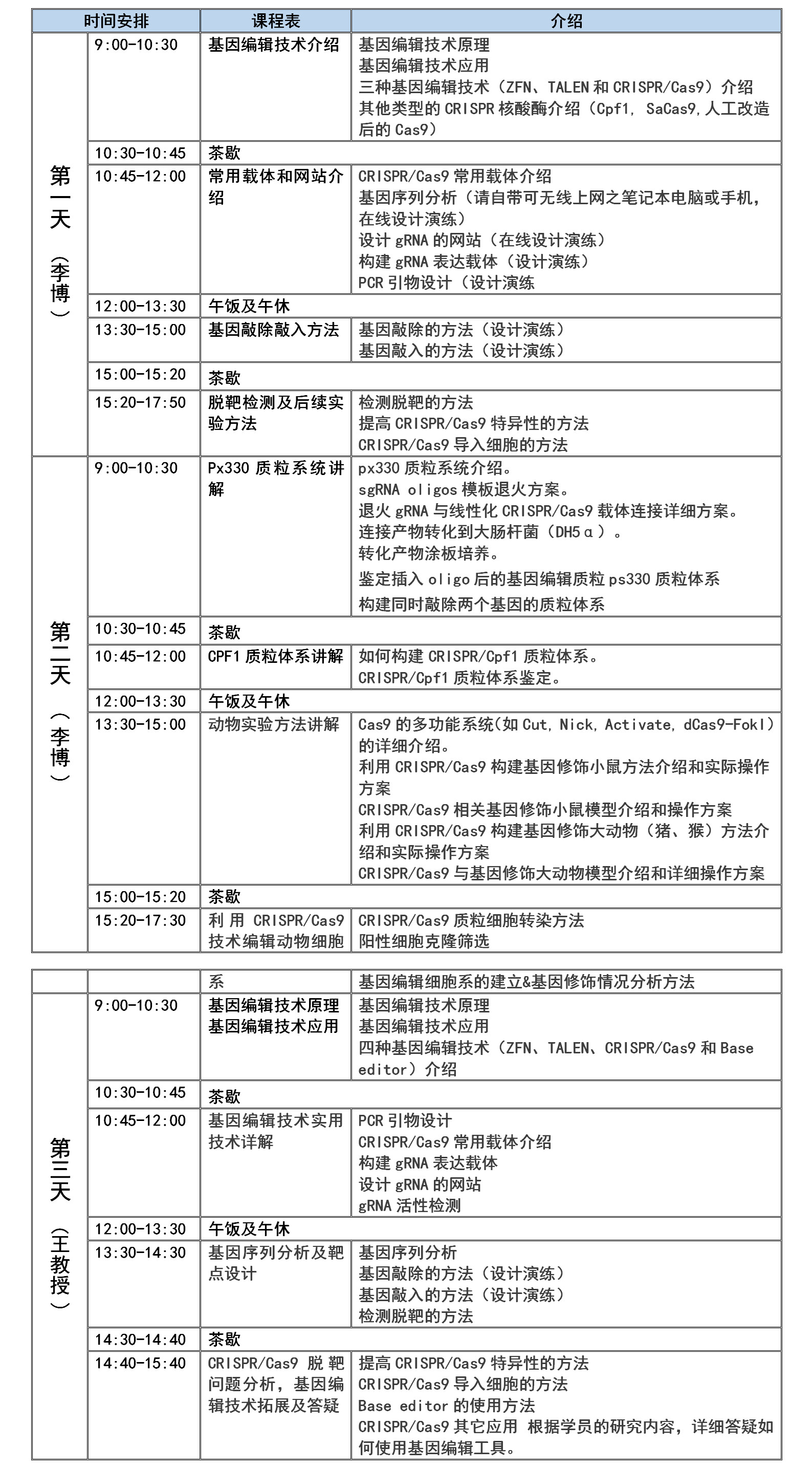
【会议日程】主要内容:
基因编辑技术介绍
常用载体和网站介绍
基因敲除敲入方法
脱靶检测及后续实验方法
Px330质粒系统讲解
CPF1质粒体系讲
动物实验方法讲解
利用CRISPR/Cas9技术编辑动物细胞
基因编辑技术原理
基因编辑技术应用
基因编辅技术实用技术详解
基因序列分析及靶点设计
CRISPR/Cas9脱靶问题分析,基因编辑技术拓展及答疑
讲师介绍:这次学习班我们邀请了两位在基因编辑领域具有丰富实操经验的教授作为主讲人,通过三天的系统学习,能让您熟悉并掌握基因编辑技术的核心知识点与详细操作技巧。
第一天与第二天主讲人:李博士
德国慕尼黑工业大学海归博士,具有多年丰富的基因编辑实操经验
参与德意志研究基金委项目(DFG)用于人类癌症研究的转基因克隆猪模型 (SCHN971/3-1)
Ø博士导师为原英国Roslin Institute克隆羊“多莉”团队的Prof. Dr. Angelika Schnieke
Ø成功构建世界上第一头ROSA26双荧光猪模型,极具有生物医学价值(已发表)。随后,成功构建Kras点突变基因修饰克隆猪模型,该模型为构建胰腺癌大动物模型提供了有力工具,为胰腺癌相关靶向药物开发,寻找新的胰腺癌治疗手段等提供了新的动物模型。
第三天主讲人:王永明教授
研究员,博士生导师,2015年国家青年千人获得者。2010-2013年在斯坦福大学医学院从事博士后研究。2013年至今历任复旦大学生命科学学院青年研究员、研究员。
王永明博士于2010年在斯坦福大学医学院做博士后研究,较早的开展了对基因编辑技术的研究和应用,主要贡献有1)首次把基因编辑技术用到了心血管领域,论文发表在Circulation Research上,被评为2012年度心脏领域最好的论文;2)首次用基因编辑技术制作了长QT综合症干细胞模型;3)发明了附着体CRISPR/Cas9技术,可以高效的敲除基因;4)发明了高通量测试gRNA效率的方法,筛选了5万多个gRNA的活性。
【会议门票】【收费标准】
注册费:3300元每位(注册费包含电子版教材、午餐,欢迎晚宴费用,住宿费自理。)
基因编辑班优惠政策:
1. 提前报名并且转账的,可以提前获取资料与发票
2. 三人组团报名,每人优惠100元
3. 四人组团报名,每人收费200元,
4. 五人组团报名缴费,额外带一人免费注册!
5. 参加免注册费复听的老学员,需缴纳600元餐费(两顿午餐,可开会务费发票,介绍新学员来的,可免除餐费)
可以开正规会务发票,纸质邀请函(盖红章)。
推荐下面三个基因编辑用的质粒可以选择订购,每个质粒800元,3个一起订购按照600元一个 (发票单独开)
1,ps330A-cas9-sgRNA(可插入任意20bp靶点序列)
2,ps330S-2-cas9-sgRNA(可用于同时敲除2个靶点的载体)
3,p-p53-cas9-GFP (可用于小鼠p53基因敲除的载体)

